一滴氯化钠(NaCl)溶液滴在热的表面上,随着水分蒸发,会出现什么现象?这个问题估计上过科学课的小学生都能回答——液滴会逐渐达到饱和,随后NaCl晶体逐渐析出。这种现象在生活中似乎再平凡不过,但是,新的科学发现有时就隐藏在这些“平凡”之中。近日,几位荷兰的科学家惊奇地发现,就在这个简单的过程背后其实还隐藏着不为人知的有趣细节——氯化钠,长出“腿”了 [1]。

“长腿”的氯化钠。图片来源:J. Phys. Chem. Lett. [1]
在聊一聊背后的原理之前,我们先来了解一下,这个简单得不能再简单的观察实验。液滴蒸发过程发生在一个硅烷化的疏水基底上,其接触角为110±4 °,温度控制在70±2 °C。在蒸发的第一阶段,NaCl溶液饱和,在液-气界面开始形成细小的微晶,并倾向于与固体表面的接触面积最小化。随着蒸发的继续,微晶逐渐长大,开始形成一个晶体网络,覆盖在液滴表面,随后才在剩余溶液的内部继续生长。当大部分水分蒸发后,剩余溶液在晶体和基底之间,析出新的微晶,并将整个晶体抬高,直到水分完全蒸发。这就是NaCl“长腿”的全过程,在晶体析出的最后一刻,NaCl仿佛基底上“站”了起来。

NaCl液滴在疏水表面蒸发的观察实验。图片来源:J. Phys. Chem. Lett. [1]
可见,液滴蒸发的最后时刻,是NaCl“长腿”的关键。研究者给出了这样的机理推测,氯化钠晶体倾向于尖角朝下,以减小其与固体表面的接触面积,这一特点在蒸发初期影响不大。但当水分剩余不多时,空气进入液-固界面,在大晶体周围的薄液膜形成了“毛细微桥”。而新的晶体在这层薄液膜内继续析出,并将之前析出的晶体网络整体抬高。
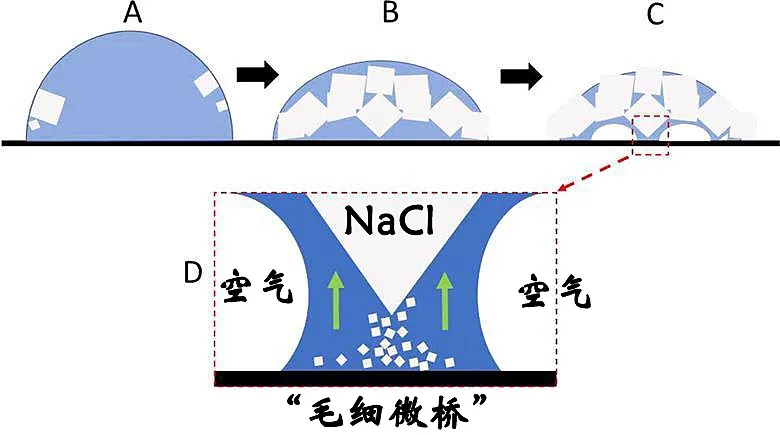
NaCl“长腿”机理示意图。图片来源:J. Phys. Chem. Lett. [1]
研究者以晶体和衬底之间的高度差(Δh),作为从上升开始到结晶结束的时间函数。基底温度对NaCl“长腿”过程的影响很大,例如在室温下(20 °C)蒸发,上升速度为0.34 μm/s,而在高温下(120 °C)蒸发,上升速度可达60 μm/s,一分钟可以上升近乎半厘米的高度。
既然是一篇严谨的科学论文,只有这个程度的解释显然是不够的。下面,要上公式了。
众所周知,阿伦尼乌斯方程表明,反应速率常数的对数(lnk),与温度的倒数(1/T)之间呈线性关系(如下),并可以用来计算反应的速率常数和活化能(详见各种版本的物理化学教材)。
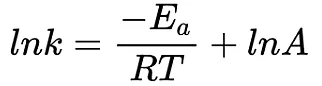
其指数形式大家可能更熟悉:
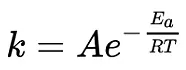
于是,研究者以lnk~1/T作图,计算出NaCl“长腿”活化能约为40 kJ/mol,这与文献报道的NaCl单晶生长的活化能(~20 kJ/mol)非常相似 [2]。不同的是,NaCl的“腿”生长于刚刚提到的“毛细微桥”中,这会导致活化能的升高。
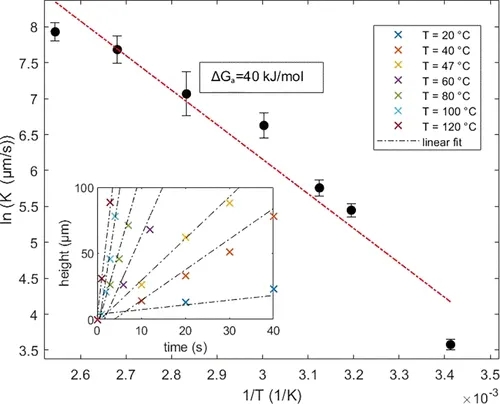
利用阿伦尼乌斯方程计算NaCl“长腿”活化能。图片来源:J. Phys. Chem. Lett. [1]
类似地,如果对KCl进行相同的实验,“长腿”活化能约为67 kJ/mol,这与文献中报道的KCl单晶生长所需的活化能(60 kJ/mol)更为接近 [3]。

KCl的“长腿”过程。图片来源:J. Phys. Chem. Lett. [1]
那么,另一个问题又来了,让NaCl“站”起来的动力来自于哪里呢?或许,是迫于结晶压力而产生的力,足以克服重力。结晶压力是晶体生长热力学的驱动力,可以用溶液的过饱和度和活度来描述。
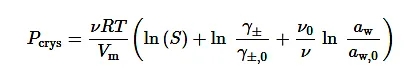
别看公式很复杂,其实活度和活度系数在实际计算时可以忽略(回忆一下我们的物化作业,好像是这样的),于是,公式瞬间简化:
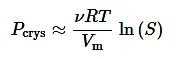
其中,S表示过饱和度。通过计算,结晶压力(Pcrys)为0.9-1.8 MPa,再利用SEM对NaCl的“腿”进行观察,估算其与基底的接触面积,不难算出结晶压力能产生大于170 mN的力,这远大于一滴液体析出的NaCl(5.2 mg)所产生的重力(51 μN),足以让NaCl晶体“站起来”。(“没有压力就没有动力”,这果然是一条颠扑不破的真理……)

SEM照片计算“腿”与基底的接触面积。图片来源:J. Phys. Chem. Lett. [1]
除了温度的影响,基底也是决定NaCl能否站起来的因素之一。出乎意料的是,除了硅烷化玻璃表面,其他超疏水基底、PDMS等材质表面,都没有出现NaCl“长腿”的奇观。这意味着,光滑的疏水表面不是NaCl长“腿”的必要条件,这一过程与基底表面与水或盐溶液的范德华力相互作用、偶极相互作用、离子相互作用、氢键和质子交换等因素都密切相关,有待进一步讨论研究。

盐水滴在三种不同表面上的蒸发实验。图片来源:J. Phys. Chem. Lett. [1]
最后,估计有人会问,研究这样一个奇怪的现象,有什么用呢?我们可能都遇到过,穿着白色鞋子踩雪,等干了之后会变得斑斑点点,这就是盐类的析出。如果这个过程因为降雨降雪发生在建筑物上,也会在墙壁上留下斑斑点点的污渍痕迹。甚至盐水渗入其中又无法排出,在内部结晶,导致建筑材料风化,造成破坏性的危险。如果可以充分理解NaCl“长腿”的机理,并加以利用,让析出的盐类晶体与材料表面的粘附最小化,从而实现材料的“自清洁”效果,或许是一条可行的思路。不过这只是研究者的大胆猜想。
无论是否有用,对于NaCl“长腿”这一现象的分析,本身就已经很有趣了,不是吗?
参考文献:
[1] Salim H. Kolpakov P. Bonn D., et al. Self-Lifting NaCl Crystals. J. Phys. Chem. Lett., 2020, 11, 7388-7393.https://pubs.acs.org/doi/10.1021/acs.jpclett.0c01871
[2] Desarnaud J. Derluyn H. Carmeliet J., et al. Growth of Salt Crystals. J. Phys. Chem. Lett., 2018, 9, 2961-2966.https://pubs.acs.org/doi/10.1021/acs.jpclett.8b01082
[3] Linnikov O. D. Spontaneous crystallization of potassium chloride from aqueous and aqueous-ethanol solutions Part 1: Kinetics and mechanism of the crystallization process. Cryst. Res. Technol., 2004, 39, 516-528.
关键词:氯化钠
分享至:
![]()
![]()




鄂公网安备 42011102004299号
© 2014-2024 前衍化学科技(武汉)有限公司 版权所有 鄂ICP备20009754号-1